این مقاله انگلیسی ISI در نشریه اسپرینگر در 8 صفحه در سال 2018 منتشر شده و ترجمه آن 14 صفحه میباشد. کیفیت ترجمه این مقاله ویژه – طلایی ⭐️⭐️⭐️ بوده و به صورت کامل ترجمه شده است.
| دانلود رایگان مقاله انگلیسی + خرید ترجمه فارسی | |
| عنوان فارسی مقاله: |
پیشرفت در ژن درمانی با ویروس واکسینای انکولیتیک به عنوان وکتور |
| عنوان انگلیسی مقاله: |
Progress in gene therapy using oncolytic vaccinia virus as vectors |
|
|
|
| مشخصات مقاله انگلیسی | |
| فرمت مقاله انگلیسی | pdf و ورد تایپ شده با قابلیت ویرایش |
| سال انتشار | 2018 |
| تعداد صفحات مقاله انگلیسی | 8 صفحه با فرمت pdf |
| نوع مقاله | ISI |
| نوع نگارش | مقاله مروری (Review Article) |
| نوع ارائه مقاله | ژورنال |
| رشته های مرتبط با این مقاله | پزشکی |
| گرایش های مرتبط با این مقاله | ژنتیک پزشکی، ویروس شناسی پزشکی |
| چاپ شده در مجله (ژورنال) | مجله تحقیقات سرطان و انکولوژی بالینی – Journal of Cancer Research and Clinical Oncology |
| کلمات کلیدی | ویروس های انکولیتیک، ویروس واکسینا، واکسن های سرطان، ژن درمانی، وکتور انکولیتیک |
| کلمات کلیدی انگلیسی | Oncolytic viruses – Vaccinia virus – Cancer vaccines – Gene therapy – Oncolytic vector |
| ارائه شده از دانشگاه | بیمارستان Wuxi People وابسته دانشگاه پزشکی نانجینگ ، بیمارستان کودکان Wuxi ، جیانگ سو ، چین |
| نمایه (index) | scopus – master journals – JCR |
| نویسندگان | Xue Yang – Biao Huang – Lili Deng – Zhigang Hu |
| شناسه شاپا یا ISSN | 0171-5216 |
| شناسه دیجیتال – doi | https://doi.org/10.1007/s00432-018-2762-x |
| ایمپکت فاکتور(IF) مجله | 4.115 در سال 2020 |
| شاخص H_index مجله | 94 در سال 2021 |
| شاخص SJR مجله | 1.338 در سال 2020 |
| شاخص Q یا Quartile (چارک) | Q2 در سال 2020 |
| بیس | نیست ☓ |
| مدل مفهومی | ندارد ☓ |
| پرسشنامه | ندارد ☓ |
| متغیر | ندارد ☓ |
| فرضیه | ندارد ☓ |
| رفرنس | دارای رفرنس در داخل متن و انتهای مقاله ✓ |
| کد محصول | 11710 |
| لینک مقاله در سایت مرجع | لینک این مقاله در سایت Springer |
| نشریه | اسپرینگر – Springer |
| مشخصات و وضعیت ترجمه فارسی این مقاله | |
| فرمت ترجمه مقاله | pdf و ورد تایپ شده با قابلیت ویرایش |
| وضعیت ترجمه | انجام شده و آماده دانلود |
| کیفیت ترجمه | ویژه – طلایی ⭐️⭐️⭐️ |
| تعداد صفحات ترجمه تایپ شده با فرمت ورد با قابلیت ویرایش | 14 (2 صفحه رفرنس انگلیسی) صفحه با فونت 14 B Nazanin |
| ترجمه عناوین تصاویر و جداول | ترجمه شده است ✓ |
| ترجمه متون داخل تصاویر | ترجمه شده است ✓ |
| ترجمه متون داخل جداول | ترجمه شده است ✓ |
| ترجمه ضمیمه | ندارد ☓ |
| ترجمه پاورقی | ندارد ☓ |
| درج تصاویر در فایل ترجمه | درج شده است ✓ |
| درج جداول در فایل ترجمه | درج شده است ✓ |
| درج فرمولها و محاسبات در فایل ترجمه | ندارد ☓ |
| منابع داخل متن | درج نشده است ☓ |
| منابع انتهای متن | به صورت انگلیسی درج شده است ✓ |
| فهرست مطالب |
|
چکیده زمینه مواد و روش ها ظهور ژن درمانی سرطان مرور کلی ویروس واکسینا مکانیسم عمل ویروس انکولیتیک در سلول های تومور دستکاری ویروس انکولیتیک ویرایش ویروس واکسینا از طریق سیستم CRISPR‑Cas9 ویروس های واکسینای حاوی ژن های درمانی به عنوان وکتورهای سرطانی ایمونوتراپیک فاکتورهای تنظیم کننده ایمنی کموکاین ها ژن های القاء کننده آپوپتوزیس ژن های سرکوب کننده تومور ژن های خودکشی مهارکننده های رگزایی خاموش کردن بیان ژن بحث نتیجه گیری منابع |
| بخشی از ترجمه |
|
چکیده زمینه: ویروس واکسینا در پروژه سازمان بهداشت جهانی برای ریشه کن کردن آبله به طور گسترده استفاده شده است و در حال حاضر این ویروس به دلیل خصوصیات منحصربفردش یک وکتور نوید بخش برای ژن درمانی است. ویروس واکسینا می تواند به صورت انتخابی همانندسازی کرده و به طور گسترده در سلول های تومور تکثیر پیدا کند که منجر به لیز شدن سلول سرطانی می شود. علاوه بر این، تولید سریع ذره ویروسی، طیف وسیع میزبان، اندازه بزرگ ژنوم (حدود 200 کیلوباز) و کنترل ایمن، ویروس واکسینا را به عنوان یک وکتور مناسب برای ژن درمانی معرفی می کند. مواد و روش ها: واکسن های سرطان و ژن درمانی اکنون تحت مطالعات بالینی و تحقیقات آزمایشگاهی قرار دارند. با این وجود، براساس تحقیقات فعلی و تجربیات فردی خودمان ما با چالش های ویژه ی انتخاب بهینه ژن های خارجی، مصرف و دستکاری VACV، ویژه سازی درمان و سایر مشکلات مواجه هستیم. نتیجه گیری: این مقاله مروری یک نگاه کلی به ویروس واکسینا از مکانیسم تا تحقیقات پزشکی و آزمایشات بالینی دارد. ما بر این باور هستیم که راه حل این مشکلات به درک مکانیسم های VACV کمک کرده و یک پایه نظری برای درمان بالینی ایجاد خواهند کرد.
زمینه راهبردهای درمان سرطان در حال حاضر یکی از نگرانی های جهانی است. سالانه نزدیک به 7 میلیون نفر به دلیل ابتلا به سرطان های بدخیم از دنیا می روند، پیش بینی می شود که در سال 2030 این عدد به 12 میلیون نفر برسد. استراتژی های اولیه درمان سرطان عبارتند از عمل جراحی، رادیوتراپی، و شیمی درمانی. با این وجود، این روش های سنتی با محدودیت هایی همراه هستند. در عمل جراحی سنتی بافت تومور به سرعت و به طور مستقیم قطع می شود، اما قطع ناقص تومور می تواند منجر به پایداری تومورهای باقیمانده شود. علاوه بر این، شیمی درمانی و رادیوتراپی اختصاصی نیستند و درکنار سلول های سرطانی سلول های ایمنی سالم را نیز از بین برده و منجر به تضعیف سیستم ایمنی بیمار می شوند. بنابراین اکنون استراتژی های هدفمند جدیدی برای غلبه بر این محدودیت ها در درمان سرطان معرفی شده اند. پیشرفت ها در مهندسی ژنتیک استفاده از وکتورهای ویروسی برای ژن درمانی سرطان را تسهیل کرده است. این استراتژی های درمانی جدید برای تومورهای بدخیم از انتقال مواد ژنتیکی خارجی به داخل سلولهای توموری از طریق وکتورهای ویروسی استفاده میکنند و به این ترتیب می توانند به طور بالقوه یک مشکل متابولیک مادرزادی، جبران حذف ژن و یا ایجاد یک عملکرد جدید را به انجام برسانند.
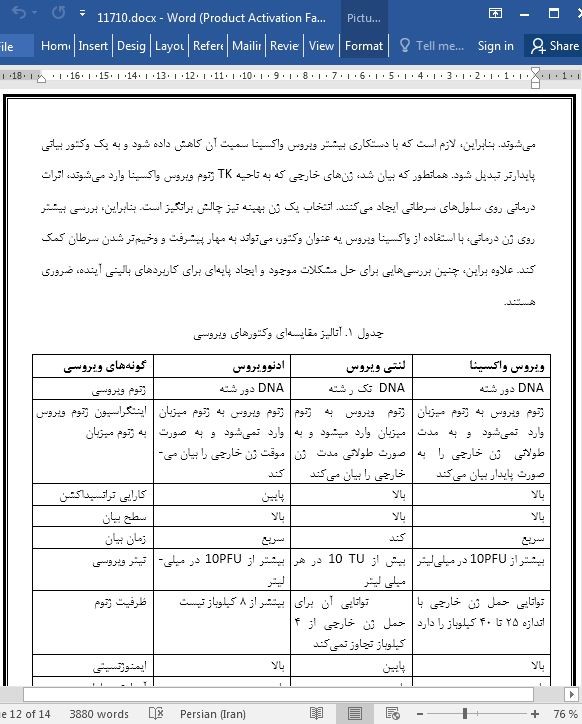
نتیجه گیری در حال حاضر بیشتر مطالعات، روی ویروس های انکولیتیک از وکتورهای آدنوویروس و لنتی ویروس به عنوان مدل استفاده می کنند؛ با این حال، مزیت های منحصربفرد ویروس واکسینا آن را به یک وکتور مناسب برای ژن درمانی تبدیل کرده است (جدول 1). رویکردهای کلی و ویژه سازی شده برای درمان بیماران مختلف مبتلا به سرطان پیشنهاد می شوند. بنابراین، لازم است که با دستکاری بیشتر ویروس واکسینا سمیت آن کاهش داده شود و به یک وکتور بیانی پایدارتر تبدیل شود. همانطور که بیان شد، ژن های خارجی که به ناحیه TK ژنوم ویروس واکسینا وارد می شوند، اثرات درمانی روی سلول های سرطانی ایجاد می کنند. انتخاب یک ژن بهینه نیز چالش برانگیز است. بنابراین، بررسی بیشتر روی ژن درمانی، با استفاده از واکسینا ویروس یه عنوان وکتور، می تواند به مهار پیشرفت و وخیم تر شدن سرطان کمک کند. علاوه براین، چنین بررسی هایی برای حل مشکلات موجود و ایجاد پایه ای برای کاربردهای بالینی آینده، ضروری هستند. |
| بخشی از مقاله انگلیسی |
|
Abstract Background Vaccinia virus was widely used in the World Health Organization’s smallpox eradication campaign and is currently a promising vector for gene therapy owing to its unique characteristics. Vaccinia virus can selectively replicate and propagate productively in tumor cells, resulting in oncolysis. In addition, rapid viral particle production, wide host range, large genome size (approximately 200 kb), and safe handling render vaccinia virus a suitable vector for gene therapy. Materials and methods Cancer vaccines and gene therapy are being studied in clinical trials and experiment researches. However, we put forward unique challenges of optimal selection of foreign genes, administration and modification of VACV, personalized medicine, and other existing problems, based on current researches and our own experiments. Conclusion This review presents an overview of the vaccinia virus from its mechanisms to medical researches and clinical trials. We believe that the solution to these problems will contribute to understanding mechanisms of VACV and provide a theoretical basis for clinical treatment.
Background Cancer treatment strategies are currently a global concern. Approximately 7 million individuals worldwide die of malignant tumors annually; this number is predicted to increase to 12 million in 2030. Primary cancer treatment strategies include surgical treatment, radiation therapy, and chemotherapy. However, these traditional treatment methods have limitations. Through traditional surgical treatment, tumor tissue can be rapidly and directly resected; however, incomplete resection may lead to the persistence of residual tumors. Furthermore, chemotherapy and radiation therapy are not target-specific; along with tumor cells, these methods also eliminate healthy immune cells, thereby lowering patient immunity. Therefore, new targeted therapeutic strategies are warranted to overcome these limitations in cancer treatment. Advancements in genetic engineering have facilitated the use of viral vectors for cancer gene therapy (Chan and Mcfadden 2014). This novel treatment strategy for malignant tumors delivers foreign genetic materials into tumor cells via viral vectors, thereby potentially rectifying congenital metabolic abnormalities, compensating for gene deletion, or facilitating a novel function.
Conclusion Currently, most studies on oncolytic viruses use adenovirus and lentiviral vectors as models; however, the unique advantages of the vaccinia virus make it a suitable vector for gene therapy (Table 1), thereby bringing hope to patients with different cancer types. Comprehensive and individualized approaches are suggested for the treatment of different patients with cancer. Therefore, there is the need to modify the vaccinia virus to reduce its toxicity level and to make it a more stable expression virus vector. As established, foreign genes integrated into the TK region of the vaccinia virus exert therapeutic effects on cancer cells. The selection of an optimal gene is also challenging. Therefore, further investigations on gene therapy, using the oncolytic vaccinia virus as a vector, could help prevent the progression and deterioration of cancer. Moreover, such investigations are very necessary for solving the existing problems, and provide the basis for future clinical applications. |
|
تصویری از مقاله ترجمه و تایپ شده در نرم افزار ورد |
|
|
| دانلود رایگان مقاله انگلیسی + خرید ترجمه فارسی | |
| عنوان فارسی مقاله: |
پیشرفت در ژن درمانی با ویروس واکسینای انکولیتیک به عنوان وکتور |
| عنوان انگلیسی مقاله: |
Progress in gene therapy using oncolytic vaccinia virus as vectors |
|
|
|