این مقاله انگلیسی ISI در نشریه ساینس دایرکت (الزویر) در 7 صفحه در سال 2011 منتشر شده و ترجمه آن 16 صفحه میباشد. کیفیت ترجمه این مقاله ویژه – طلایی ⭐️⭐️⭐️ بوده و به صورت کامل ترجمه شده است.
| دانلود رایگان مقاله انگلیسی + خرید ترجمه فارسی | |
| عنوان فارسی مقاله: |
رفتارهای ساختاری 1.7 دی اکسا – اسپیرو (5.5) اندسان و ساختارهای مشابه دییتیا و دیسلنا در رابطه با اثر آنومریک: بررسی هیبرید DFT و تحلیل تفاسیر NBO و روش ab initio |
| عنوان انگلیسی مقاله: |
Conformational behaviors of 1,7-dioxa-spiro[5,5]undecane and its dithia and diselena analogs in relation to the anomeric effect: A hybrid-DFT, ab initio MO study and NBO interpretation |
|
|
|
| مشخصات مقاله انگلیسی | |
| فرمت مقاله انگلیسی | |
| سال انتشار | 2011 |
| تعداد صفحات مقاله انگلیسی | 7 صفحه با فرمت pdf |
| نوع مقاله | ISI |
| نوع نگارش | مقاله پژوهشی (Research Article) |
| نوع ارائه مقاله | ژورنال |
| رشته های مرتبط با این مقاله | شیمی |
| گرایش های مرتبط با این مقاله | شیمی کاربردی، شیمی آلی و شیمی محض |
| چاپ شده در مجله (ژورنال) | شیمی محاسباتی و نظری – Computational and Theoretical Chemistry |
| کلمات کلیدی | اثرات آنومریک، NBO ، مدل سازی مولکولی، 1.7 دی اکسا – اسپیرو (5.5) اندسان |
| کلمات کلیدی انگلیسی | Anomeric effects – NBO – Molecular modeling – 1.7-Dioxa-spiro[5.5]undecane |
| ارائه شده از دانشگاه | گروه شیمی، شعبه اراک، دانشگاه آزاد اسلامی، ایران |
| نمایه (index) | Scopus – Master journals – JCR |
| نویسندگان | Davood Nori-Shargh، Hooriye Yahyaei، Seiedeh Negar Mousavi، Mina Kianpour |
| شناسه شاپا یا ISSN | ISSN 2210-271X |
| شناسه دیجیتال – doi | https://doi.org/10.1016/j.comptc.2011.07.014 |
| ایمپکت فاکتور(IF) مجله | 1.359 در سال 2019 |
| شاخص H_index مجله | 82 در سال 2020 |
| شاخص SJR مجله | 0.418 در سال 2019 |
| شاخص Q یا Quartile (چارک) | Q3 در سال 2019 |
| بیس | نیست ☓ |
| مدل مفهومی | ندارد ☓ |
| پرسشنامه | ندارد ☓ |
| متغیر | ندارد ☓ |
| رفرنس | دارای رفرنس در داخل متن و انتهای مقاله ✓ |
| کد محصول | 10523 |
| لینک مقاله در سایت مرجع | لینک این مقاله در نشریه Elsevier |
| نشریه الزویر |  |
| مشخصات و وضعیت ترجمه فارسی این مقاله | |
| فرمت ترجمه مقاله | pdf و ورد تایپ شده با قابلیت ویرایش |
| وضعیت ترجمه | انجام شده و آماده دانلود |
| کیفیت ترجمه | ویژه – طلایی ⭐️⭐️⭐️ |
| تعداد صفحات ترجمه تایپ شده با فرمت ورد با قابلیت ویرایش | 16 صفحه با فونت 14 B Nazanin |
| ترجمه عناوین تصاویر و جداول | ترجمه شده است ✓ |
| ترجمه متون داخل تصاویر | ترجمه شده است ✓ |
| ترجمه متون داخل جداول | ترجمه شده است ✓ |
| درج تصاویر در فایل ترجمه | درج شده است ✓ |
| درج جداول در فایل ترجمه | درج شده است ✓ |
| درج فرمولها و محاسبات در فایل ترجمه | به صورت عکس درج شده است ✓ |
| منابع داخل متن | به صورت عدد درج شده است ✓ |
| منابع انتهای متن | به صورت انگلیسی درج شده است ✓ |
| فهرست مطالب |
|
چکیده |
| بخشی از ترجمه |
|
1- مقدمه ترکیبات اشباع شده هتروسایکلی در برگیرنده یک بخش بزرگ از شیمی آلی و غیر آلی می باشند و در طبیعت بسیار پراکنده هستند ( برای نمونه ، در الکالوئیدها – کربوهیدرات ها – تنظیم کننده رشد گیاه و غیره ) . کسب اطلاعات در مورد تاثیرات واکنش های استروالکترونی و استری بر ویژگی های های ساختاری ترکیبات هتروسایکلی علاقه مندان زیادی به خود جلب کرده است.
4- نتیجه گیری محاسبات هیبرید ΔFT که در بالا گزارش شده اند ، همراه با تجزیه و تحلیل NBO ، تصویری منطقی از چشم اندازهای ساختاری ، انرژی ، پیوندی و استروالکتریکی در ترکیبات 3-1 ارائه می کنند. نتایج مربوط به B3LYP/6-311+G نشان می دهند که مقادیر ΔGC–B و ΔGB–A , ΔGC–A محاسبه شده از ترکیب 1 تا ترکیب 3 کاهش می یابند. روند مشابهی برای مقادیر محاسبه شده AEC–B, AEB–A , AEC–A مشاهده می شود. متعاقبا ، همبستگی بین AE ومقادیر ΔGC–B, ΔGB–A و ΔGC–A محاسبه شده از نظر AE تا جایی پیش می رود که اولویت تشکیل ساختار A برای ترکیبات در نظر گرفته شود (3-1). نکته مهم این است که اختلاف برای ΔlC–B, ΔlB–A محاسبه شده و ΔlC–A از ترکیب 1 تا ترکیب 3 برای ساختارهای ΔGC–B, ΔGB–A و ΔGC–A هم مشاهده می شود. بنابراین ، همبستگی منطقی بین اختلاف زمان دو قطبی و اختلاف نهایی انرژی یافت نمی شود. |
| بخشی از مقاله انگلیسی |
|
1- Introduction The saturated heterocyclic compounds comprise a large segment of organic and inorganic chemistry and are quite widespread in nature (e.g., in alkaloids, carbohydrates, plant growth regulators, etc.), the knowledge about the impacts of the stereoelectronic, steric and electrostatic interactions on the conformational properties of heterocyclic compounds is of very general interest.
4- Conclusion The above reported hybrid-DFT calculations and NBO analysis provided a reasonable picture from structural, energetic, bonding and stereoelectronic points of view for the conformational behavior in compounds 1–3. Effectively, B3LYP/6-311+G results revealed that the calculated DGC–B, DGB–A and DGC–A values decrease from compound 1 to compound 3. Similar trend is observed for the calculated AEC–B, AEB–A and AEC–A values. Accordingly, the correlation between the AE and the calculated DGC–B, DGB–A and DGC–A values is strong enough. Consequently, the rationalization of the conformational preference solely in terms of the AE succeeds to account for conformation A preference of compounds 1–3. Importantly, the variations of the calculated DlC–B, DlB–A and DlC–A values from compound 1 to compound 3 are not in the same trend observed for the corresponding DGC–B, DGB–A and DGC–A values. Therefore, a reasonably correlation between the dipole moment differences and total energy differences was not found. |
|
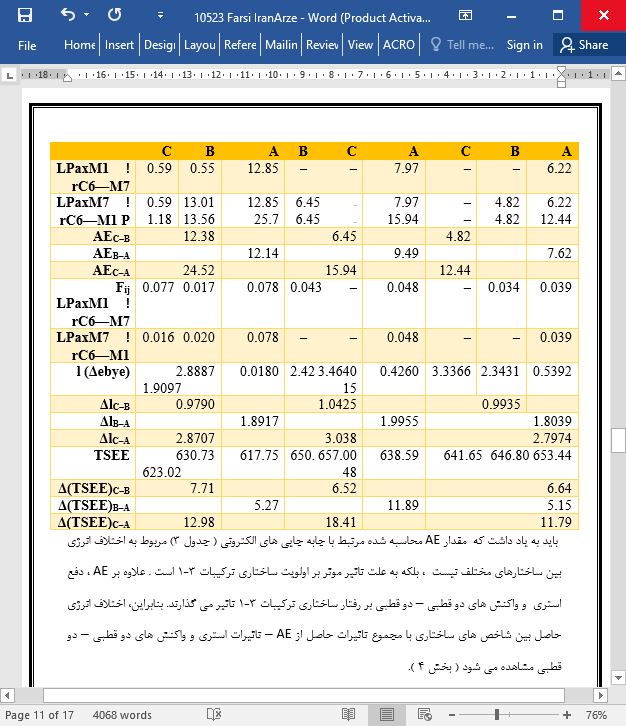
تصویری از مقاله ترجمه و تایپ شده در نرم افزار ورد |
|
|
| دانلود رایگان مقاله انگلیسی + خرید ترجمه فارسی | |
| عنوان فارسی مقاله: |
رفتارهای ساختاری 1.7 دی اکسا – اسپیرو (5.5) اندسان و ساختارهای مشابه دییتیا و دیسلنا در رابطه با اثر آنومریک: بررسی هیبرید DFT و تحلیل تفاسیر NBO و روش ab initio |
| عنوان انگلیسی مقاله: |
Conformational behaviors of 1,7-dioxa-spiro[5,5]undecane and its dithia and diselena analogs in relation to the anomeric effect: A hybrid-DFT, ab initio MO study and NBO interpretation |
|
|
|